
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-11-26 05:36.
- Viimati modifitseeritud 2025-01-22 16:57.
l = 3 f alamkesta jaoks. Orbitaalide arv on = 2l+1=7. See mahutab kokku 14 elektroni. Seega on peakvantarvuga n=4 kesta jaoks olemas 16 orbitaali , 4 alamkihti, 32 elektroni (maksimaalselt) ja 14 elektroni, mille l=3.
Samuti on küsimus, mitu orbitaali on n 4-s?
16 orbitaali
Seejärel tekib küsimus, mitut tüüpi orbitaale on kestas, mille aatomis on N4? ja iga ml väärtus vastab ühele orbitaal . Meil on 4 − sel juhul alamkestad; s, p, d, f ↔ 0, 1, 2, 3 jaoks l väärtus. =16−− orbitaalid = 4 − energiatase. Kui kordate protsessi jaoks n =3, leiaksite lmax=2 ja seal on 9− orbitaalid in =3−.
Mitu orbitaali on N 5 kestas?
5. jaoks kest , = 5 . = jaoks 5 , l-i lubatud väärtused on 0, 1, 2, 3 ja 4 (l-1). 1+3+ 5 +7+9 = 25 orbitaalid . Võite kasutada ka järgmist võrrandit: number of orbitaalid = n².
Mitu orbitaali on N 2 kestas?
neli
Soovitan:
Mitu EcoRI saiti on lambda DNA-s?
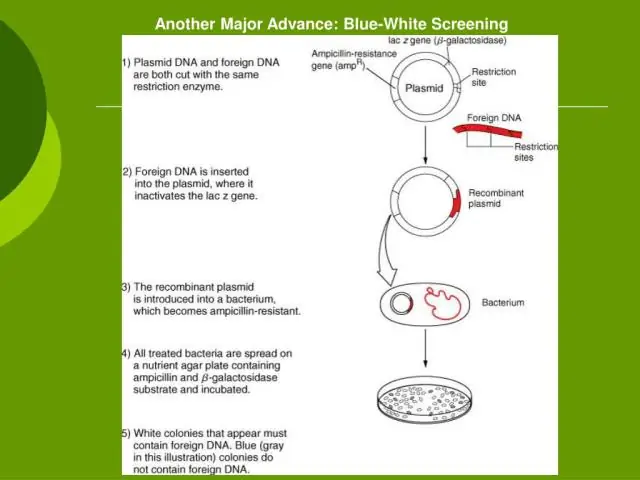
Selles katses kasutatud lambda DNA eraldatakse lineaarse molekulina E. coli lambda bakteriofaagist. See sisaldab ligikaudu 49 000 aluspaari ja sellel on 5 tuvastuskohta Eco RI ja 7 Hind III jaoks
Mitu orbitaali on viiendal põhienergiatasemel?

Esimene kvantarv: orbitaalide ja elektronide arvutused Iga energiataseme jaoks on n2 orbitaali. Kui n = 1, on orbitaal 12 või üks. Kui n = 2, on 22 või neli orbitaali. Kui n = 3 on üheksa orbitaali, n = 4 korral on 16 orbitaali, n = 5 korral on 52 = 25 orbitaali ja nii edasi
Mitu orbitaali on M kestas?

M kest mahutab ainult kaheksa elektroni. M-kest mahutab tegelikult kuni 18 elektroni, kui liigute kõrgemate aatomarvude poole. Maksimaalne elektronide arv mis tahes kestast on 32
Kuidas sa tead, mitu orbitaali on kestas?

Orbitaalide arv kestas on peakvantarvu ruut: 12 = 1,22 = 4, 32 = 9. On üks orbitaali s alamkestas (l = 0), kolm orbitaali ap alamkoores (l = 1) ja viis orbitaali reklaami alamkestas (l = 2). Orbitaalide arv alamkoores on seega 2(l) +1
Mitu orbitaali on kestas, mille n 5 on?

Kui n = 3 on üheksa orbitaali, n = 4 korral on 16 orbitaali, n = 5 korral on 52 = 25 orbitaali ja nii edasi
