
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:35.
- Viimati modifitseeritud 2025-01-22 16:57.
The aatomi raadius kemikaalist element on kaugus tuuma keskpunktist elektroni välimise kihini.
Samuti küsivad inimesed, kus on perioodilisuse tabeli aatomiraadius?
Aatomiraadiuste tabel
| Aatomnumber | Elemendi sümbol | Aatomiraadius [Å] |
|---|---|---|
| 10 | Ne | 0.38 |
| 11 | Na | 1.90 |
| 12 | Mg | 1.45 |
| 13 | Al | 1.18 |
Seejärel tekib küsimus, milline on mangaani aatomiraadius? Elementide aatomiraadius
| Heelium | 31 õhtul | 161 õhtul |
|---|---|---|
| Raud | 156 õhtul | 231 õhtul |
| Indium | 156 õhtul | 233 õhtul |
| Tallium | 156 õhtul | 238 õhtul |
| Mangaan | 161 õhtul | 243 õhtul |
Mis on siin elemendi raadius?
Aatomi raadius Aatomi (r) võib defineerida poolena kaheaatomilise molekuli kahe tuuma vahelisest kaugusest (d). Aatomiline raadiused on mõõdetud elementide jaoks. Aatomi ühikud raadiused on pikomeetrid, võrdne 10-ga−12 meetrit.
Milleks kasutatakse aatomiraadiust?
See termin kirjeldab an Atom - Aga see pole täpne D. Aatomi raadius on termin harjunud kirjeldage an suurust aatom . Selle väärtuse jaoks pole aga standarddefinitsiooni. The aatomi raadius võib viidata ioonsele raadius , kovalentne raadius , metallist raadius või van der Waals raadius.
Soovitan:
Milline on elemendi väikseim osake, mis säilitab elemendi omadused?

Aatom on mis tahes elemendi väikseim osake, mis säilitab endiselt selle elemendi omadused. Osa elemendist, mida me suudame näha või käsitseda, koosneb paljudest, paljudest aatomitest ja kõik aatomid on ühesugused, neil kõigil on sama arv prootoneid
Mis on keskpunkt ja raadius?
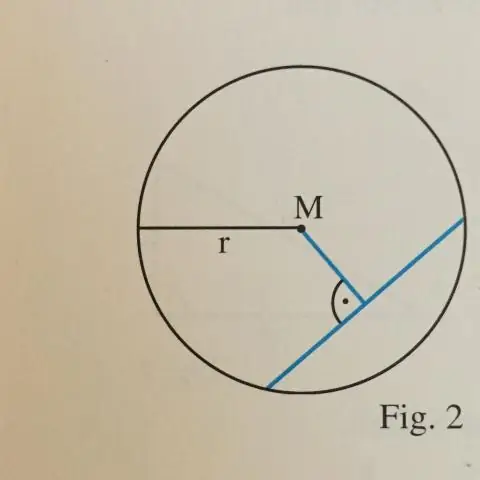
Ringvõrrandi keskpunkti raadiuse vorm on formaadis (x – h)2 + (y – k)2 = r2, kus keskpunkt asub punktis (h, k) ja raadius on 'r'. See võrrandi vorm on kasulik, kuna saate hõlpsalt leida keskpunkti ja raadiuse
Mitu elektroni on iga elemendi aatomi teisel energiatasemel?

Kui esimesel energiatasemel on 2 elektroni, lähevad järgmised elektronid teisele energiatasemele, kuni teisel tasemel on 8 elektroni. Kui teisel energiatasemel on 8 elektroni, lähevad järgmised elektronid kolmandale energiatasemele, kuni kolmandal tasemel on 8 elektroni
Kuidas aatomi raadius suureneb?

Selle põhjuseks on prootonite ja elektronide arvu suurenemine perioodi jooksul. Ühel prootonil on suurem mõju kui ühel elektronil; seega tõmmatakse elektronid tuuma poole, mille tulemuseks on väiksem raadius. Aatomi raadius suureneb rühma sees ülalt alla. Selle põhjuseks on elektronide varjestus
Kus on perioodilisuse tabeli aatomi suurus?

Perioodilise tabeli suundumusi aitavad ennustada kolm tegurit: prootonite arv tuumas, kestade arv ja varjestusefekt. Aatomi suurus suureneb mis tahes rühmas ülalt alla kõigi kolme teguri suurenemise tulemusena
